An transplante alogénico de células nai é un tratamento intensivo no que recibe un transplante de células nai do doador (outra persoa). Isto é diferente a cando un paciente recibe as súas propias células de volta, o que se chama un transplante autólogo de células nai. Isto é discutido noutra páxina.
Visión xeral dos transplantes aloxénicos de células nai?
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital
O transplante de células nai aloxénicas utiliza células nai recollidas dun doador (outra persoa) para substituír as súas propias células nai. Isto faise para tratar o linfoma que é refractario (que non responde ao tratamento) ou que é recurrente (linfoma que segue volvendo. A maioría das persoas con linfoma non necesitan un transplante de células nai. No linfoma, os transplantes aloxénicos (doadores) son moito máis raros que os autólogos ( auto) transplantes.
O linfoma é un cancro de linfocitos. Os linfocitos son un tipo de glóbulos brancos que se desenvolven a partir de células nai. O obxectivo de quimioterapia é erradicar as células de linfoma e todas as células nai que potencialmente poderían converterse en linfoma. Unha vez que se erradican as células malas, poden volver crecer células novas que esperamos que non sexan cancerosas.
No caso das persoas que teñen un linfoma en recaída ou refractario, isto non funciona; máis linfoma segue crecendo a pesar do tratamento. Polo tanto, a erradicación das células nai con doses moi altas de quimioterapia e, a continuación, substituír as células nai desa persoa polas doutra persoa pode dar lugar a un novo sistema inmunitario no que as células nai doadores asumen o papel de producir células sanguíneas que non se converten en linfoma.
O obxectivo dun transplante de células nai
Hai unha serie de razóns polas que os pacientes con linfoma poden necesitar un transplante de células nai que inclúen:
- Para tratar pacientes con linfoma que están en remisión, pero teñen un "alto risco" de que regrese o seu linfoma
- O linfoma volveu despois do tratamento inicial estándar de primeira liña, polo que se usa unha quimioterapia máis intensa (máis forte) para recuperar a remisión (sen enfermidade detectable)
- O linfoma é refractario (non respondeu completamente) ao tratamento estándar de primeira liña co obxectivo de lograr unha remisión.
O transplante de células nai aloxénicas pode realizar dúas funcións
- As doses moi altas de quimioterapia eliminan o linfoma e as novas células doadores proporcionan un xeito de recuperar o sistema inmunitario, reducindo o tempo que o sistema inmunitario está fóra de acción. As novas células doadoras asumen o papel da función do sistema inmunitario e da produción de células sanguíneas sans, como os linfocitos. As células nai do doador substitúen ás células nai disfuncionais do paciente.
- Efecto enxerto versus linfoma. Isto é cando as células nai doadoras (chamadas enxerto) recoñecen as células de linfoma restantes e as atacan, destruíndo o linfoma. Este é un efecto positivo onde as células nai do doador están axudando a tratar o linfoma. É importante ter en conta que este efecto enxerto versus linfoma non sempre ocorre así. O linfoma pode ser resistente ás células nai do doador ou o corpo do receptor (chamado hóspede) pode loitar contra as células do doador (chamado enxerto) enfermidade do enxerto contra o hóspede (complicación do transplante aloxénico).
O proceso dun transplante aloxénico de células nai ten cinco etapas
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital
- Preparación: isto inclúe análises de sangue para determinar o tipo de células que precisa. Ás veces, as persoas precisan recibir quimioterapia de "salvamento" para tratar de minimizar o linfoma antes do transplante.
- Colección de células nai: este é o proceso de recolección de células nai, porque un transplante aloxénico é dun doador, o equipo médico necesita atopar unha coincidencia para o transplante.
- Tratamento acondicionador: esta é a quimioterapia, terapia diana e inmunoterapia que se administra en doses moi altas para eliminar todo o linfoma.
- Reinfusión de células nai: unha vez administrados os tratamentos de alta dose, adminístrase as células nai que previamente foron recollidas do doador.
- Enxerto: este é o proceso polo cal as células nai doadores se instalan no corpo e asumen o funcionamento do sistema inmunitario.
Preparación para o tratamento
Haberá moita preparación necesaria antes do transplante de células nai. Cada transplante é diferente e o equipo de transplantes debe organizalo todo para o paciente. Algúns dos preparativos que cabe esperar poden incluír:
A inserción dunha liña central
Se o paciente aínda non ten unha liña central, entón inserirase unha antes do transplante. Unha liña central pode ser un PICC (catéter central inserido periféricamente). Podería ser unha CVL (liña venosa central). O médico decidirá que liña central é mellor para o paciente.
A liña central proporciona unha forma de recibir moitos medicamentos diferentes ao mesmo tempo. Os pacientes xeralmente necesitan moitos medicamentos diferentes e análises de sangue durante o transplante e unha liña central axuda ás enfermeiras a xestionar mellor o coidado do paciente.
quimioterapia
A quimioterapia en doses altas sempre se administra como parte do proceso de transplante. Chámase quimioterapia en doses altas terapia condicionante. Fóra da quimioterapia de alta dose, algúns pacientes necesitan quimioterapia de rescate. A terapia de salvamento é cando o linfoma é agresivo e debe reducirse antes de que o resto do proceso de transplante poida continuar. O nome salvamento vén de intentar salvar o corpo do linfoma.
Reubicación para tratamento
Só certos hospitais de Australia son capaces de realizar transplantes de células nai aloxénicas. Debido a isto, pode ter que mudarse da súa casa a unha zona máis próxima ao hospital. A maioría dos hospitais de transplantes teñen aloxamento para pacientes no que poden vivir o paciente e o seu coidador. Fale co traballador social do teu centro de tratamento para coñecer as opcións de aloxamento.
Conservación da fertilidade
O transplante de células nai afectará a capacidade do paciente para ter fillos. É importante que se discutan as opcións dispoñibles para preservar a fertilidade.
Consellos prácticos
O transplante de células nai normalmente implica unha longa estancia hospitalaria. Pode ser útil empaquetar algunhas destas cousas:
- Varios pares de roupa ou pixamas suaves e cómodos e moita roupa interior.
- Cepillo de dentes (suave), pasta de dentes, xabón, hidratante suave, desodorante suave
- A túa propia almofada (lave en quente a funda de almofada e as mantas persoais/alfombras antes do ingreso no hospital: lavalas en quente para reducir as bacterias xa que o teu sistema inmunitario será moi vulnerable).
- Pantuflas ou zapatos cómodos e moitos pares de calcetíns
- Artigos persoais para alegrar o teu cuarto de hospital (unha foto dos teus seres queridos)
- Elementos de entretemento como libros, revistas, crucigramas, iPad/portátil/tableta. O hospital pode ser moi aburrido se non tes nada que facer.
- Un calendario para facer un seguimento da data, os ingresos hospitalarios longos poden difuminar todos os días xuntos.
HLA e tipificación de tecidos
Cando se realiza un transplante de células nai aloxénicas (doadores), o coordinador de transplantes organiza a busca dun doador de células nai axeitado. É máis probable que un transplante de células nai aloxénicas teña éxito se as células do doador coinciden moito co paciente. Para comprobar isto, o paciente farase unha análise de sangue chamada tipificación de tecidos que observa diferentes proteínas na superficie das células chamadas antíxenos leucocitarios humanos (HLA).
As células de todos producen proteínas HLA para axudar ao sistema inmunitario a recoñecer as células que pertencen ao corpo e recoñecer as células que non pertencen.
Hai moitos tipos diferentes de HLA e o equipo médico trata de atopar un doador cuxos tipos de HLA coincidan o máis parecido posible.
Se é posible, tamén tratan de asegurarse de que o paciente e o doador estiveron expostos aos mesmos virus, aínda que isto é menos importante que a coincidencia de HLA.
É máis probable que os irmáns ou irmás teñan proteínas HLA similares ás do paciente. Ao redor de 1 de cada 3 persoas ten un irmán ou unha irmá que é unha boa parella. Se un paciente non ten irmáns ou irmás, ou se non son unha boa parella, o equipo médico buscará un doador voluntario cuxo tipo de HLA se axuste o máis posible aos pacientes. Isto coñécese como un doador non relacionado (MUD) e millóns de voluntarios están rexistrados nos rexistros de células nai nacionais e globais.
Se non se atopa un doador non relacionado (MUD) compatible para o paciente, pode ser posible utilizar outras fontes de células nai. Estes inclúen:
- Un familiar cuxa metade tipo HLA coincide coa túa: coñécese como doador "haploidéntico".
- Sangue de cordón umbilical dun doador non relacionado: o sangue de cordón umbilical non ten que coincidir tanto co seu tipo de HLA como outras fontes de células nai. É máis probable que se use para nenos que para adultos porque contén menos células nai que outras fontes. Están dispoñibles os rexistros de sangue do cordón umbilical almacenado.
Colección de células nai
Hai dúas formas en que un doador pode doar células nai.
- Recolección de células nai do sangue periférico
- Doazón de células nai do sangue de medula ósea
Doazón de células nai de sangue periférico
As células nai periféricas recóllense do torrente sanguíneo periférico. Antes da recollida de células nai periféricas, a maioría das persoas reciben inxeccións de factor de crecemento. Os factores de crecemento estimulan a produción de células nai. Isto axuda ás células nai a pasar da medula ósea ao torrente sanguíneo, listas para a súa recollida.
A recollida ocorre separando as células nai do resto do sangue e o proceso utiliza unha máquina de aférese. Unha máquina de aférese pode separar diferentes compoñentes do sangue e pode separar as células nai. Unha vez que o sangue pasou pola fase de recollida celular, volve ao corpo. Este proceso leva varias horas (aproximadamente 2-4 horas). O doador pode volver a casa despois do procedemento, non obstante, pode ter que regresar ao día seguinte se non se recolleron suficientes células.
A aférese é menos invasiva que a recollida de medula ósea e por iso é en parte o motivo polo que é o método preferido de recollida de células nai.
Nos transplantes aloxénicos (doadores), o doador é sometido a aférese para o receptor e esta recollida realízase o máis preto posible do día do transplante. Porque estas células nai serán entregadas frescas ao receptor o día do transplante.
Doazón de células nai do sangue de medula ósea
O método menos común para recoller células nai é a colleita de medula ósea. Aquí é onde as células nai son retiradas da medula ósea baixo anestesia xeral. Os médicos introducen unha agulla nun óso da rexión pélvica, chamada crista ilíaca. A medula ósea é retirada da pelve, a través da agulla e esta medula ósea é despois filtrada e almacenada ata o día do transplante.
Sangue do cordón umbilical a doazón procede do banco público de cordón, onde se doou e almacenou unha doazón de células nai do sangue que queda no cordón umbilical e a placenta despois do nacemento dun bebé.
Como funciona a aférese
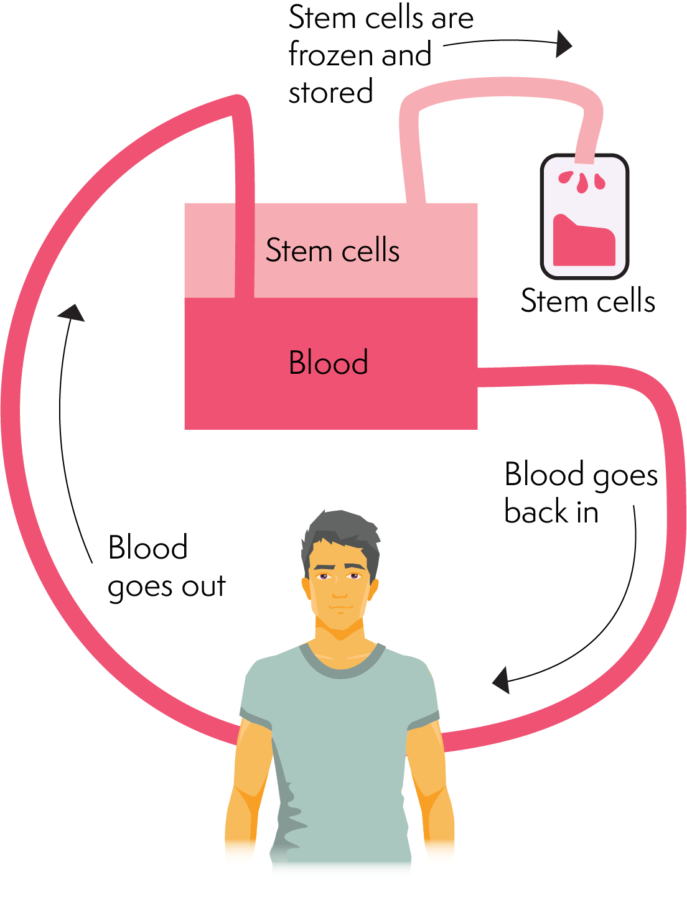
Procesamento/preservación das células nai ou da medula ósea
As células nai recollidas para transplante aloxénico (doador) recóllense inmediatamente antes do seu uso e non se almacenan durante ningún período de tempo.
As células nai recollidas para (auto)transplante autólogo, xeralmente consérvanse e almacénanse nun conxelador ata que estean listas para o seu uso.
Condicionamentos
Os pacientes sometidos a un transplante reciben primeiro un tratamento denominado réxime de acondicionamento. Este é un tratamento de alta dose que se administra nos días anteriores á infusión das células nai. A terapia de acondicionamento pode incluír quimioterapia e ás veces radioterapia. Os dous obxectivos da terapia de acondicionamento son:
- Para matar o máximo de linfoma posible
- Reducir a poboación de células nai
Hai moitas combinacións diferentes de quimioterapia, radioterapia e inmunoterapia que se poden usar en réximes de acondicionamento. Hai diferentes intensidades de tratamento de acondicionamento, son:
- Acondicionamento mieloablativo de plena intensidade
- Acondicionamento non mieloablativo
- Acondicionamento de intensidade reducida
En todos os réximes o tratamento é intensivo e, como resultado, moitas células sans morren xunto co linfoma. A elección do réxime dependerá do tipo de linfoma, o historial de tratamento e outros factores individuais, como a idade, a saúde xeral e a forma física. O equipo de tratamento discutirá co paciente cal é o réxime de acondicionamento adecuado para o paciente.
Nun transplante aloxénico, os pacientes poden ingresar no hospital xa 14 días antes do transplante. Cada caso do paciente é diferente e o seu médico informarache de cando será ingresado. Os pacientes permanecen no hospital entre 3 e 6 semanas despois do transplante. Esta é unha pauta; cada transplante é diferente e algunhas persoas necesitan máis atención médica durante máis de 6 semanas.
Se está a ter un transplante de células nai aloxénicas utilizando células nai dun doador importante ou non relacionado, é posible que necesite un tratamento de acondicionamento de maior intensidade.
Pode ter un tratamento de acondicionamento diferente se está a ter un transplante aloxénico usando células nai de sangue do cordón umbilical ou dun parente semi-pareado.
Podes acceder a información detallada sobre réximes de acondicionamento no Páxina web de Eviq.
Reinfusión de células nai
Despois de que a quimioterapia intensiva de acondicionamento rematou, as células nai son reinfundidas. Estas células nai comezan lentamente a producir novas células sanguíneas saudables. Finalmente, producirán suficientes células sans para repoboar toda a medula ósea, repoñendo todas as células sanguíneas e inmunes.
Reinfundir as células nai é un procedemento sinxelo. É semellante a unha transfusión de sangue. As células son introducidas a través dunha liña na liña central. O día en que se reinfunden as células nai denomínase "Día Cero".
Con calquera procedemento médico, existe o risco de ter unha reacción á infusión de células nai. Para a maioría da xente non hai reaccións, pero outros poden experimentar:
- Sentirse enfermo ou estar enfermo
- Mal gusto ou sensación de ardor na boca
- Tensión alta
- Reacción alérxica
- Infección
Nos transplantes de células nai aloxénicas, xa que estas células doadas se afianzan (ou enxertan) no receptor (paciente). Comezan a funcionar como parte do sistema inmunitario e poden atacar as células do linfoma. Isto chámase efecto enxerto versus linfoma.
Nalgúns casos, despois do transplante aloxénico, as células doadoras tamén atacan as células sans do paciente. Isto chámase enfermidade de enxerto contra hóspede (GVHD).
Enxerto das súas células nai
O enxerto é cando as novas células nai comezan a tomar o relevo gradualmente como células nai primarias. Isto xeralmente ocorre entre 2 e 3 semanas despois da infusión de células nai, pero pode levar máis tempo, especialmente se as novas células nai proceden de sangue do cordón umbilical.
Mentres as novas células nai se enxertan, ten un risco moi alto de contraer unha infección. As persoas xeralmente teñen que permanecer no hospital durante este período, porque poden enfermarse e necesitan recibir tratamento de inmediato.
Mentres estás esperando a que mellore o teu reconto sanguíneo, podes ter algúns dos seguintes tratamentos para apoiar a túa recuperación:
- Transfusións de sangue: para o reconto baixo de glóbulos vermellos (anemia)
- Transfusións de plaquetas: para niveis baixos de plaquetas (trombocitopenia)
- Antibióticos - para infeccións bacterianas
- Medicamento antiviral - para infeccións virais
- Medicamento antifúngico - para infeccións fúngicas
Síndrome do enxerto
Despois de recibir as novas células nai, algunhas persoas desenvolven os seguintes síntomas 2-3 semanas despois, xeralmente no momento do enxerto celular:
- Febre: temperatura alta de 38 graos ou máis
- Unha erupción vermella
- Diarrea
- Retención de líquidos
Isto chámase "síndrome de enxerto". É máis común despois dun autotransplante de células nai (autólogo) que dun transplante de células nai de doantes (aloxénicos).
É un efecto secundario común do transplante e trátase con esteroides. Estes síntomas tamén poden ser causados por outros factores, incluíndo a quimioterapia, e poden non ser un sinal de síndrome de enxerto.
Algúns protocolos hospitalarios comúns durante un transplante inclúen:
- Normalmente permanece nunha habitación de hospital pola súa conta durante a duración da súa estadía
- A habitación do hospital límpase regularmente e cámbianse as sabas e as fundas de almofadas todos os días
- Non podes ter plantas ou flores vivas no teu cuarto
- O persoal do hospital e os visitantes deben lavarse as mans antes de entrar na súa habitación
- Ás veces, os visitantes e o persoal do hospital poden ter que usar luvas, batas ou mandil e máscaras faciais cando te visiten
A xente non debe visitarche se non está ben - Os nenos menores dunha determinada idade poden non poder visitar en absoluto, aínda que algúns hospitais permítenllo se os nenos están ben
Unha vez que se recuperou o seu reconto sanguíneo e o paciente estea o suficientemente ben, pode volver a casa. Transcorrido este tempo, serán seguidos de cerca polo equipo médico.
Complicacións do transplante de células nai
Enfermidade de enxerto contra hóspede (GvHD)
A enfermidade do enxerto contra o hóspede (GvHD) é unha complicación común dun transplante de células nai aloxénicas. Ocorre cando:
- As células T doadoras (tamén chamadas "enxerto") recoñecen os antíxenos doutras células do corpo do receptor (chamadas "hóspede") como estrañas.
- Despois de recoñecer estes antíxenos, as células T doadoras atacan as células do seu novo hóspede.
Este efecto pode ser útil cando os novos linfocitos T doadores atacan as células de linfoma restantes (chamado efecto enxerto versus linfoma). Desafortunadamente, as células T doadores tamén poden atacar os tecidos sans. Isto pode causar efectos secundarios graves.
Na maioría das veces, a GvHD causa síntomas de leves a moderados, pero ás veces pode ser grave e incluso ameazar a vida. Antes e despois do transplante, os pacientes reciben tratamento para reducir o risco de desenvolver GvHD. O equipo de transplantes monitoriza de preto o paciente para detectar calquera signo de GvHD para que poida tratalo o antes posible, se se desenvolve.
A GvHD clasifícase como "aguda" ou "crónica", dependendo dos signos e síntomas.
Risco de infección
Despois dun transplante de células nai, as altas doses de quimioterapia eliminarán moitos glóbulos brancos, incluído un glóbulo branco chamado neutrófilos. Un nivel baixo de neutrófilos coñécese como neutropenia. A neutropenia prolongada pon a alguén en un risco moi alto de desenvolver unha infección. As infeccións poden ser tratadas, pero se non se detectan pronto e se tratan inmediatamente, poden poñer en perigo a vida.
Mentres estea no hospital, inmediatamente despois do transplante de células nai, o equipo de tratamento tomará precaucións para evitar o desenvolvemento de infeccións, así como un seguimento de cerca para detectar sinais de infección. Aínda que se toman moitas precaucións para reducir o risco de contraer unha infección, a maioría dos pacientes que teñen un transplante de células nai aloxénicas contraerán unha infección.
Nas primeiras semanas despois do transplante, os pacientes corren o maior risco de desenvolver unha infección bacteriana. Tales infeccións inclúen, infeccións do torrente sanguíneo, pneumonía, infeccións do sistema dixestivo ou infeccións da pel.
Nos próximos meses, os pacientes corren o maior risco de desenvolver infeccións virais e estes poden ser virus que estaban latentes no corpo antes do transplante e que poden estalar cando o sistema inmunitario está baixo. Non sempre causan síntomas. Realizaranse análises de sangue regulares despois do transplante para asegurarse de que se detecta precozmente un brote dunha infección viral chamada citomegalovirus (CMV). Se unha análise de sangue mostra a presenza de CMV, aínda que non teña síntomas, o paciente terá tratamento con medicamentos antivirais. Pode ser necesario máis dun curso de tratamento e este tratamento pode prolongar a estancia hospitalaria.
Os recontos sanguíneos comezan a aumentar entre 2 e 4 semanas despois dun transplante de células nai aloxénicas. Non obstante, o sistema inmunitario pode tardar moitos meses, ou ás veces incluso anos, en recuperarse completamente.
Ao ser dado de alta do hospital, o equipo médico debe indicar cales son os signos de infección a ter en conta e con quen contactar se existe unha posible infección ou calquera outra cousa que poida ser unha preocupación para o paciente.
Efectos secundarios da quimioterapia en doses moi altas
É probable que os pacientes experimenten efectos secundarios do tratamento contra o cancro de altas doses. Os seguintes efectos secundarios poden ser comúns e hai máis información no efectos secundarios sección
- Mucosite oral (dolor na boca)
- Anemia (conto baixo de glóbulos vermellos)
- Trombocitopenia (conto baixo de plaquetas)
- Náuseas e vómitos
- Problemas do tracto dixestivo (diarrea ou estreñimiento)
Fallo do enxerto
O fracaso do enxerto ocorre se as células nai transplantadas non se instalan na medula ósea e producen novas células sanguíneas. Isto significa que os recontos sanguíneos non se recuperan, ou comezan a recuperarse pero despois baixan de novo.
O fracaso do enxerto é grave, pero é raro despois dun transplante de células nai aloxénicas, especialmente se o doador é un bo partido.
O equipo médico supervisará de cerca os recontos sanguíneos e se a nova célula nai comeza a fallar, o paciente pode ser tratado inicialmente con hormonas do factor de crecemento. Estes poden fomentar que as células nai da medula ósea produzan máis células.
Se as células nai do doador non se enxertan, o paciente pode necesitar un segundo transplante de células nai. Este segundo transplante pode ser do mesmo doador de células nai ou doutro diferente.
Efectos tardíos
Os efectos tardíos son problemas de saúde que poden desenvolverse meses ou anos despois do tratamento do linfoma. A maioría dos centros de transplantes teñen dedicados servizos de efectos tardíos que ofrecen programas de detección para detectar efectos tardíos o antes posible. Isto dálle ao paciente as mellores posibilidades de ser tratado con éxito se desenvolve algún efecto tardío.
Os pacientes tamén poden estar en risco de desenvolver un trastorno linfoproliferativo posttransplante (PTLD), linfomas que poden desenvolverse en persoas que están tomando fármacos inmunosupresores despois dun transplante. Non obstante, o PTLD é raro. A maioría dos pacientes que tiveron transplantes non desenvolven PTLD.
Atención de seguimento
Despois dun transplante de células nai, haberá citas regulares (semanais) co médico. O seguimento continuará durante meses e anos despois do tratamento, pero cada vez con menos frecuencia a medida que pasa o tempo. Finalmente, os médicos transplantados poderán entregar os coidados de seguimento ao médico de cabeceira do paciente.
Aproximadamente 3 meses despois dun transplante, a PET scan, Tomografía computarizada e / ou aspirado de medula ósea (BMA) pode programarse para avaliar como vai a recuperación.
É habitual ter que volver ao hospital para recibir tratamento nas semanas e meses posteriores a un transplante, pero a medida que pasa o tempo, o risco de complicacións graves diminúe.
Tamén é probable que os pacientes experimenten efectos secundarios do tratamento con doses altas e poidan sentirse mal e moi cansos. Non obstante, normalmente leva ao redor dun ano recuperarse dun transplante de células nai.
O equipo médico debe aconsellar sobre outros factores a considerar durante o período de recuperación. Lymphoma Australia ten unha páxina privada en Facebook en liña, Lymphoma Down Under, onde podes facer preguntas e obter apoio doutras persoas afectadas por un linfoma ou un transplante de células nai.
Que pasa despois dun transplante de células nai?
Tratamento de acabado pode ser un momento difícil para moitos pacientes, xa que se readaptan á vida despois do transplante. Algunhas das preocupacións comúns poden estar relacionadas con:
- físico
- Benestar mental
- Saúde emocional
- Relación
- Traballo, estudo e actividades sociais
Máis información
A Steve foi diagnosticado con linfoma de células do manto en 2010. Steve sobreviviu a un transplante de células nai autólogo e aloxénico. Esta é a historia de Steve.
Dr Nada Hamad, hematóloga e médica de transplante de medula ósea
Hospital de San Vicente, Sydney
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital
Dr Amit Khot, hematólogo e médico en transplante de medula ósea
Peter MacCallum Cancer Center e Royal Melbourne Hospital

